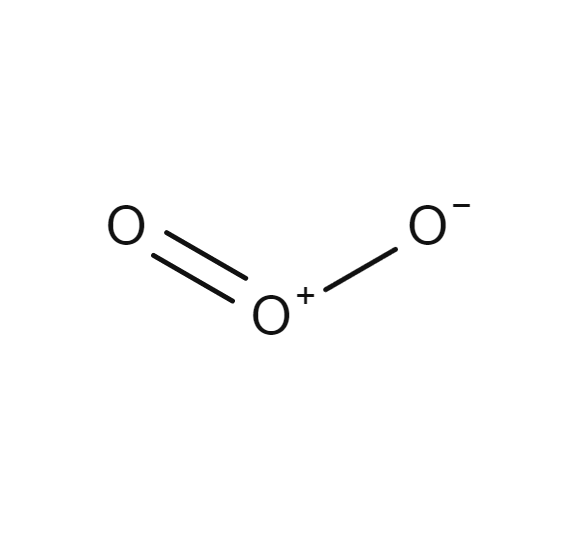
Ozone
- O3
- Numéro CAS 10028-15-6
Cliquez et faites tourner la molécule 3D
Volumes Gaz / Liquide
Calculer le volume ou la masse d'une quantité de gaz ou de liquide
Phase Liquide
Au point d'ébullition à 1,013 bar
Phase Gazeuse
Dans les conditions standard (1,013 bar, 15°C)
Propriétés physiques
Diagramme de phase moléculaire montrant les phases de transition entre le solide, le liquide et le gaz en fonction de la température et de la pression
-
- Masse molaire 47.998 g/mol
- Teneur dans l'air sec /
-
Point critique
- Température -12.15 °C
- Pression 55,7 bar
- Masse volumique 539.31 kg/m³
-
Point triple
- Température -193.00 °C
- Pression 7,346E-6 bar
Pression 1.013 bar
| Chaleur latente de fusion (au point de fusion) | 41,668 kJ/kg |
| Point de fusion | - 193 °C |
Pression 1.013 bar
| Point d'ébullition | - 111,3 °C |
| Chaleur latente de vaporisation (au point d'ébullition) | 288,49 kJ/kg |
| Masse volumique du liquide (au point d'ébullition) | 1349,08 kg/m3 |
| Equivalent gaz/(liquide au point d'ébullition) | 626,31 vol/vol |
| Conductivité thermique | 17,889 mW/(m.K) |
| Viscosité | 1,3923E-4 Po |
| Equivalent gaz/(liquide au point d'ébullition) | 626,31 vol/vol |
| Conductivité thermique | 19,068 mW/(m.K) |
| Viscosité | 1,4569E-4 Po |
| Equivalent gaz/(liquide au point d'ébullition) | 626,31 vol/vol |
| Conductivité thermique | 19,854 mW/(m.K) |
| Viscosité | 1,4996E-4 Po |
Candidatures
Des exemples d'utilisations de la molécule dans l'industrie et la santé

Composants électroniques
L'ozone est utilisé comme oxydant pour le dépot des oxydes dans le procédé de dépôt de couches atomiques assisté ou non par plasma (PE) ALD. L'ozone est utilisé dans certaines étapes de nettoyage des wafers.

Gestion des déchets et de l'eau
L'ozone est utilisé dans le traitement des eaux pour décomposer certains polluants (par oxydation), réduire les odeurs et décolorer les effuents. L'ozone peut également être utilisé pour le blanchiment et consitue une alternative respectueuse de l'environnement aux produits chlorés, en tant qu'agent biocide.

Alimentaire
L'ozone permet la désinfection des eaux utilisées pour la pisciculture, la production alimentaire et l'assainissement.

Autre
L'eau ozonée est utilisée pour la désinfection des surfaces et des produits. L'ozone est utilisé pour les piscines, les spas, la neutralisation des odeurs, etc.

Pharma & Biotechnologie
L'ozone est utilisé comme réactif dans les procédés de synthèse chimique et de traitement des eaux usées.

Pâte à papier
L'ozone permet un blanchiment de la pâte à papier selon un procédé plus respectueux de l'environnement. L'ozone est utilisé pour réduire les résidus fluorescents issus des azurants optiques dans le traitement des déchets papiers. L'ozone intervient lors du traitement de certains effluents.
Sécurité & Compatibilité
GHS03
Comburant
GHS05
Corrosif
GHS06
Toxique ou mortel
Seuil de toxicité
| PEL USA OSHA (vol) | 0,1 ppm |
| VLEP 8h France (à Patm et 293.15 K) | 0,2 mg/m3 ou 0,1 ppm |
| VLEP CT France (à Patm et 293.15 K) | 0,4 mg/m3 ou 0,2 ppm |
Métaux
| Aluminium | Pas de données |
| Laiton | Pas de données |
| Alliage de Nickel | Pas de données |
| Cuivre | Pas de données |
| Aciers ferritiques | Pas de données |
| Aciers inoxydables | Pas de données |
| Zinc | Pas de données |
| Titane | Pas de données |
Plastiques
| Polytétrafluoroéthylène | Pas de données |
| Polychlorotrifluoroéthylène | Pas de données |
| Polyfluorure de vinylidène | Pas de données |
| Polychlorure de vinyle | Pas de données |
| Ethylène tétrafluoroéthylène | Pas de données |
| Polycarbonate | Pas de données |
| Polyamide | Pas de données |
| Polypropylène | Pas de données |
Elastomères
| Caoutchouc (isobutène- isoprène) butyl | Pas de données |
| Caoutchouc nitrile butadiène | Pas de données |
| Chloroprène | Pas de données |
| Chlorofluorocarbones | Pas de données |
| Silicone | Pas de données |
| Perfluoroélastomères | Pas de données |
| Fluoroélastomères | Pas de données |
| Néoprène | Pas de données |
| Polyuréthane | Pas de données |
| Ethylène-Propylène | Pas de données |
Lubrifiants
| Huile de lubrification à base d'hydrocarbures | Pas de données |
| Huile de lubrification à base de fluorocarbures | Pas de données |
Compatibilité avec les matériaux
En savoir plus
En savoir plus
L'ozone a été découvert en 1789 par Martin van Marum, cependant Christian Friedrich Schönbein est considéré comme le père de l'ozone. Son nom vient du mot grec « ozein », signifiant « exhaler les odeurs », « sentir ». L'ozone est formé par la combinaison de trois atomes d'oxygène. Gaz instable à l'odeur forte et irritante (ce qui explique son nom), l'ozone est corrosif, puissamment oxydant et très toxique. En règle générale, la production d'ozone s'effectue par la production de décharges électriques à haute tension dans l'air ou l'oxygène. A l'état naturel, on le trouve dans les couches supérieures de l'atmosphère, où il se forme par réaction photochimique. L'ozone y joue un rôle de bouclier protégeant notre planète contre les rayons ultraviolets du soleil.